
我校麻醉学院名誉院长安建雄教授团队丘脑痛机制研究取得新进展,首次发现ADCY1蛋白表达变化与丘脑痛的发病及电针治疗相关,为今后探究丘脑痛发病机制和治疗方法提供了新的线索。该研究获国家自然科学基金和科技部重大专项基金资助,并由我校麻醉学院以及附属医院麻醉与睡眠医学中心、美国匹兹堡大学麻醉学系、中国医科大学航空总医院、中国科学院北京转化医学研究院、中国科学院大学等科研院所合作完成。在安建雄教授指导下,其在读博士研究生马宝丰关于电针治疗丘脑痛疗效和机制的成果被刊登在最新一期美国介入疼痛医师官方杂志《Pain Physician》。
丘脑痛,又称卒中后中枢痛,是一种严重的中枢神经病理性疼痛,因为发病机制不清,治疗十分困难。丘脑痛病人极为痛苦,也给家庭和社会带来沉重负担。安建雄教授博士研究生、我校麻醉学院校友张建峰首先建立了新型蛇毒型丘脑痛模型,随后利用这一模型开展各种干预及机制研究,发现几乎所有现有药物均无济于事,而电针和经颅磁呈现出显著疗效。其中安建雄教授的在读博士研究生马宝丰关于电针治疗丘脑痛疗效和机制的成果被刊登在最新一期美国介入疼痛医师官方杂志《Pain Physician》。

安建雄团队发现电针可通过抑制ADCY1蛋白表达增高缓解大鼠丘脑痛,近日发表在美国介入疼痛医师杂志官方杂志Pain Physician
研究人员将实验用大鼠分为三组,分别为假手术组、丘脑痛组和电针组。丘脑痛组大鼠于右侧丘脑腹后外侧核注入眼镜蛇毒1μL,而假手术组则注入等量生理盐水,电针组是在成功建立大鼠丘脑痛模型之后,每隔一日对右侧“曲池”和“手三里”穴位进行电针刺激30分钟,并每七天进行一次机械回缩阈值检测及行为学录像观察,以发现各组大鼠痛阈变化。至术后28天治疗结束后处死大鼠,取术侧丘脑进行生物信息学及分子生物学检测分析。
结果发现,与假手术组相比,丘脑痛组有858个基因表达上调,255个基因表达下调;与丘脑痛组相比,电针组有229个基因表达上调,148个基因表达下调;进行多组间筛选分析发现,有71个基因在丘脑痛组表达上调而在电针组下调,41个基因在丘脑痛组表达下调而在电针组上调。这些基因位于不同的细胞组分,具有不同的分子功能,参与不同的生物过程,影响不同的信号通路。通过GO、KEGG以及蛋白相互作用网络分析发现,腺苷酸环化酶亚型1(ADCY1)可能是电针治疗丘脑痛过程中的关键差异表达蛋白,该蛋白的表达变化可能影响丘脑痛的发生、发展和电针治疗过程。实时荧光定量PCR检测、免疫印迹实验和免疫荧光实验结果均表明,与假手术组相比,丘脑痛组ADCY1表达升高,而电针治疗之后,ADCY1表达回调至基本正常。
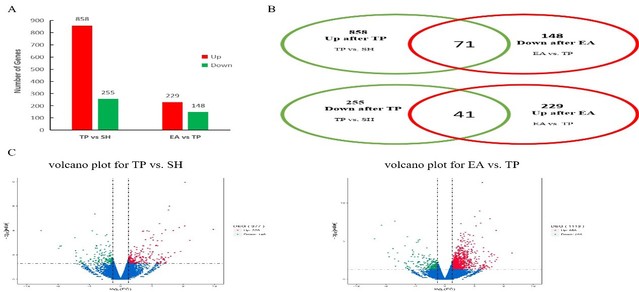
不同组别基因表达差异示意图
ADCY1是N-甲基-D-天冬氨酸(NMDA)受体的主要下游信号蛋白,并被认为是治疗慢性疼痛的潜在新靶点。以往研究报道,ADCY1在动物疼痛模型中显著促进行为敏化和脊髓易化;ADCY1可诱导长时程增强并触发疼痛的传递和感知;ADCY1抑制剂(ST034307)能够降低cAMP生成、蛋白激酶A(PKA)激活和前扣带回皮质中的NMDA受体表达,从而治疗慢性疼痛;鞘内注射ADCY1的抑制剂(NB001)可以缓解糖尿病神经病变引起的严重神经病理性疼痛。
该研究首次发现ADCY1蛋白表达变化与丘脑痛的发病及电针治疗相关。因为ADCY1只在中枢神经系统表达,作者认为电针作用于丘脑痛大鼠的外周穴位可引起神经中枢相关蛋白表达发生变化,进而可能影响疼痛传导通路,最后达到减轻疼痛的效果。该研究为今后探究丘脑痛发病机制和治疗方法提供了新的线索。